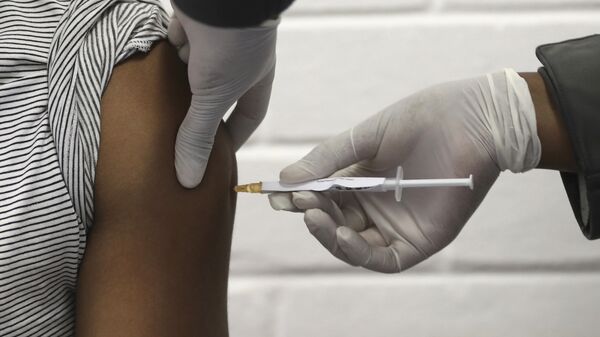
A Agência Nacional de Vigilância Sanitária (Anvisa) destacou que, segundo os regulamentos nacionais e internacionais de Boas Práticas Clínicas, os dados sobre voluntários de pesquisas clínicas "devem ser mantidos em sigilo, em conformidade com princípios de confidencialidade, dignidade humana e proteção dos participantes".
De acordo com a agência, a notificação sobre o falecimento brasileiro foi feita em 19 de outubro. A Anvisa não informou se o voluntário brasileiro que participou dos testes tomou a vacina ou o placebo.
"É importante ressaltar que, com base nos compromissos de confidencialidade ética previstos no protocolo, as agências reguladoras envolvidas recebem dados parciais referentes à investigação realizada por esse comitê, que sugeriu pelo prosseguimento do estudo. Assim, o processo permanece em avaliação", declarou a agência.
Já o Instituto D’Or de Pesquisa e Ensino (Idor), que é responsável pelos testes no Rio de Janeiro, declarou que "após a inclusão de mais de 20 mil participantes nos testes ao redor do mundo, todas as condições médicas registradas foram cuidadosamente avaliadas pelo comitê independente de segurança, pelas equipes de investigadores e autoridades regulatórias locais e internacionais".
"A análise rigorosa dos dados colhidos até o momento não trouxe qualquer dúvida com relação à segurança do estudo, recomenda-se sua continuidade. Vale lembrar que se trata de um estudo randomizado e cego, no qual 50% dos voluntários recebem o imunizante produzido por Oxford. No Brasil, até o presente momento, já foram vacinados aproximadamente 8.000 voluntários", disse o instituto, citado pelo O Globo.