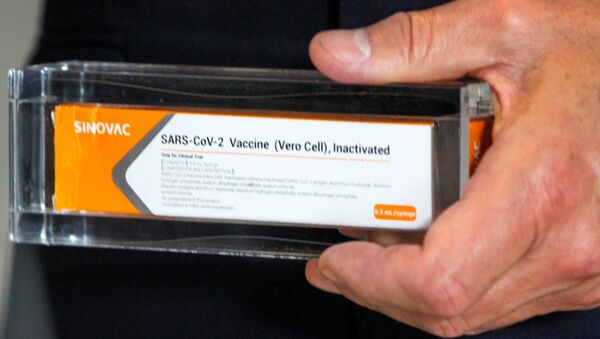
Em nota, a agência diz que a interrupção foi feita após ter sido notificada sobre a ocorrência de um "Evento Adverso Grave".
"Após ocorrência de Evento Adverso Grave a Anvisa determinou a interrupção do estudo clínico da vacina Coronavac. O evento ocorrido no dia 29/10 foi comunicado à Anvisa, que decidiu interromper o estudo para avaliar os dados observados até o momento e julgar sobre o risco/benefício da continuidade do estudo", escreveu a Anvisa.
A partir desse momento, nenhum novo voluntário brasileiro poderá ser vacinado.
"Os dados sobre voluntários de pesquisas clínicas devem ser mantidos em sigilo, em conformidade com princípios de confidencialidade, dignidade humana e proteção dos participantes", disse a agência.
Segundo a Anvisa, são considerados Eventos Adversos Graves:
- óbito;
- evento adverso potencialmente fatal (aquele que, na opinião do notificante, coloca o indivíduo sob risco imediato de morte devido ao evento adverso ocorrido);
- incapacidade/invalidez persistente ou significativa;
- exige internação hospitalar do paciente ou prolonga internação;
- anomalia congênita ou defeito de nascimento;
- qualquer suspeita de transmissão de agente infeccioso por meio de um dispositivo médico;
- evento clinicamente significante.
A CoronaVac estava na terceira e última fase de testes. Com a interrupção, ela se torna agora a terceira vacina contra COVID-19 que teve seus ensaios clínicos suspensos por efeitos adversos graves.
O imunizante contra o novo coronavírus desenvolvido pela Universidade de Oxford teve seus testes interrompidos após uma voluntária apresentar sintomas de uma doença neurológica. Já a vacina da Johnson & Johnson também interrompeu os testes depois de uma "doença inexplicada" ter acometido um dos participantes.