https://noticiabrasil.net.br/20240108/anvisa-aprova-vacina-indiana-contra-covid-19-32429707.html
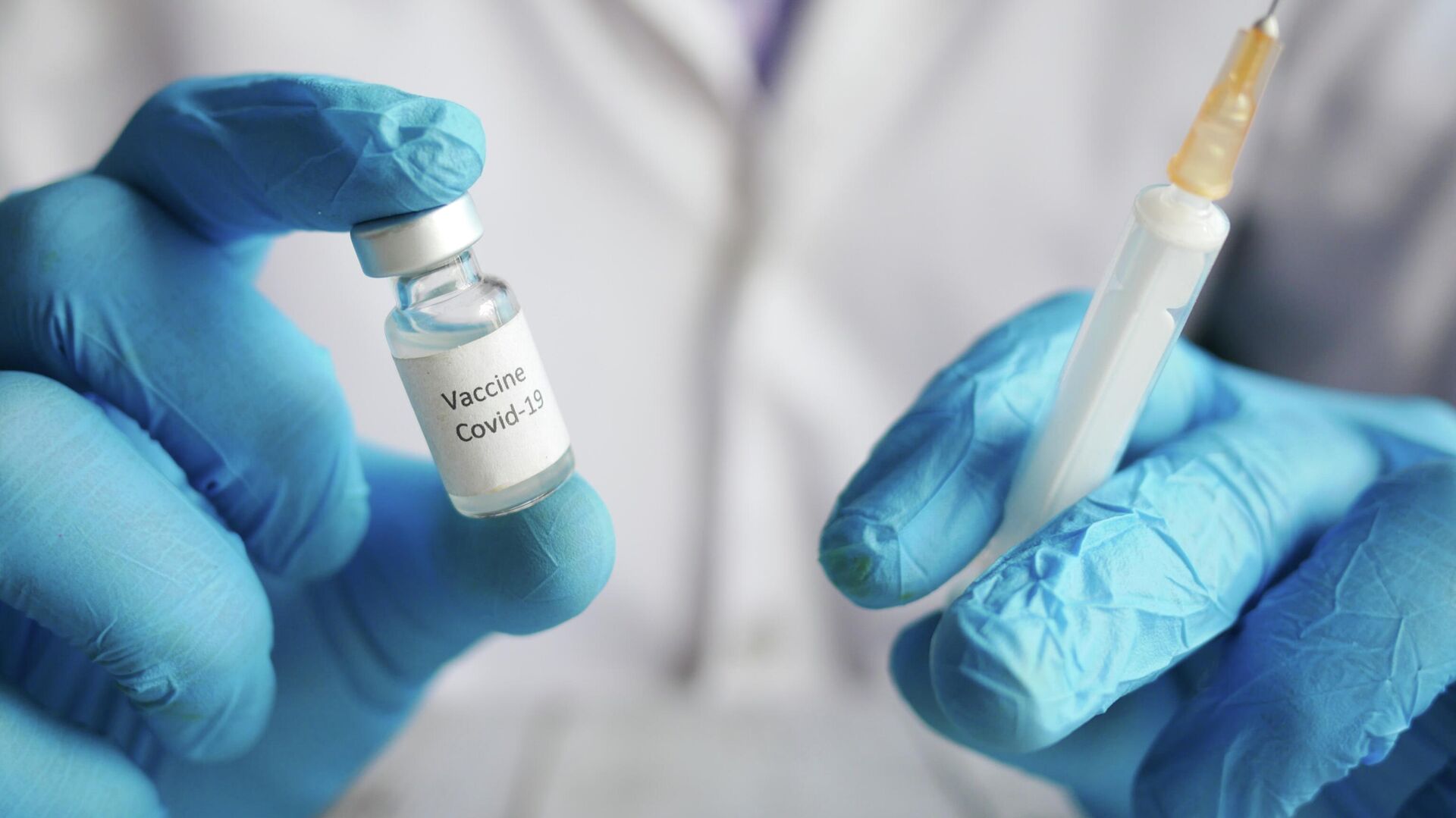
Anvisa aprova vacina indiana contra COVID-19
Anvisa aprova vacina indiana contra COVID-19
Sputnik Brasil
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou nesta segunda-feira (8) o registro da vacina para COVID-19 solicitado pela empresa Zalika... 08.01.2024, Sputnik Brasil
2024-01-08T16:23-0300
2024-01-08T16:23-0300
2024-01-08T20:49-0300
notícias do brasil
ásia e oceania
mundo
anvisa
brasil
covid-19
vacina
oms
organização mundial da saúde (oms)
imunizante
https://cdn.noticiabrasil.net.br/img/07e8/01/08/32429410_0:304:3069:2030_1920x0_80_0_0_c1da29e76ded6623fb0ef3118bac8643.jpg
A vacina usa tecnologia de proteína recombinante, com adjuvante à base de saponina, e permite produzir dentro da indústria o material que será utilizado para gerar a formação de anticorpos no organismo.Duas doses serão necessárias, e a segunda deve ser administrada 21 dias após a primeira. A Anvisa recomenda, ainda, a dose de reforço da vacina aproximadamente seis meses após a imunização primária — para indivíduos com 18 anos ou mais.De acordo com a agência, após a avaliação do Ministério da Saúde, poderá ser incorporada ao Programa Nacional de Imunizações (PNI).A Anvisa informou que um dos estudos avaliou a eficácia da vacina em população adulta nos Estados Unidos e no México e apresentou eficácia de 90,4% para a prevenção da COVID-19. No Reino Unido, esse percentual chegou a 89,7%.Seguindo as orientações da Organização Mundial da Saúde (OMS), a Anvisa realizará alterações de processo fabril e buscará apresentar provas e dados complementares para a demonstração da manutenção da segurança e eficácia da vacina atualizada. A alteração do processo e a apresentação do novo conjunto de dados, explica o órgão, é condição para a manutenção do registro, conforme o termo de compromisso firmado entre a agência e a empresa, com prazo para atendimento ainda no início de 2024.
https://noticiabrasil.net.br/20240105/bndes-anuncia-investimento-de-r-30-milhoes-em-vacina-contra-covid-19-da-fiocruz-32402035.html
brasil
reino unido
méxico
estados unidos
Sputnik Brasil
contato.br@sputniknews.com
+74956456601
MIA „Rossiya Segodnya“
2024
Sputnik Brasil
contato.br@sputniknews.com
+74956456601
MIA „Rossiya Segodnya“
notícias
br_BR
Sputnik Brasil
contato.br@sputniknews.com
+74956456601
MIA „Rossiya Segodnya“
Sputnik Brasil
contato.br@sputniknews.com
+74956456601
MIA „Rossiya Segodnya“
ásia e oceania, mundo, anvisa, brasil, covid-19, vacina, oms, organização mundial da saúde (oms), imunizante, doença, vírus, pandemia, ministério da saúde, agência nacional de vigilância sanitária, reino unido, méxico, estados unidos, eua, ciência, saúde
ásia e oceania, mundo, anvisa, brasil, covid-19, vacina, oms, organização mundial da saúde (oms), imunizante, doença, vírus, pandemia, ministério da saúde, agência nacional de vigilância sanitária, reino unido, méxico, estados unidos, eua, ciência, saúde
Anvisa aprova vacina indiana contra COVID-19
16:23 08.01.2024 (atualizado: 20:49 08.01.2024) A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou nesta segunda-feira (8) o registro da vacina para COVID-19 solicitado pela empresa Zalika Farmacêutica, que representa no Brasil o Instituto de Soro da Índia. O imunizante será usado para a prevenção da doença em pessoas a partir de 12 anos de idade.
A vacina usa
tecnologia de proteína recombinante, com adjuvante à base de saponina, e permite produzir dentro da indústria o material que será utilizado para
gerar a formação de anticorpos no organismo.
Duas doses serão necessárias, e a segunda deve ser administrada 21 dias após a primeira. A Anvisa recomenda, ainda, a dose de reforço da vacina aproximadamente seis meses após a
imunização primária — para indivíduos com 18 anos ou mais.
De acordo com a agência, após a avaliação do Ministério da Saúde, poderá ser
incorporada ao Programa Nacional de Imunizações (PNI).
A Anvisa informou que um dos estudos avaliou a eficácia da vacina em população adulta nos Estados Unidos e no México e apresentou eficácia de 90,4% para a prevenção da COVID-19. No Reino Unido, esse percentual chegou a 89,7%.
"Os dados clínicos apresentados também permitiram concluir que a vacina possui perfil de segurança aceitável, e a totalidade das informações apresentadas demonstraram que os benefícios da utilização da vacina COVID-19 (recombinante) para a prevenção da doença superam os riscos", diz o informativo da Anvisa.
Seguindo as orientações da
Organização Mundial da Saúde (OMS), a Anvisa realizará alterações de processo fabril e buscará apresentar provas e dados complementares para a demonstração da manutenção da segurança e eficácia da vacina atualizada. A alteração do processo e a apresentação do novo conjunto de dados, explica o órgão, é
condição para a manutenção do registro, conforme o termo de compromisso firmado entre a agência e a empresa, com
prazo para atendimento ainda no início de 2024.